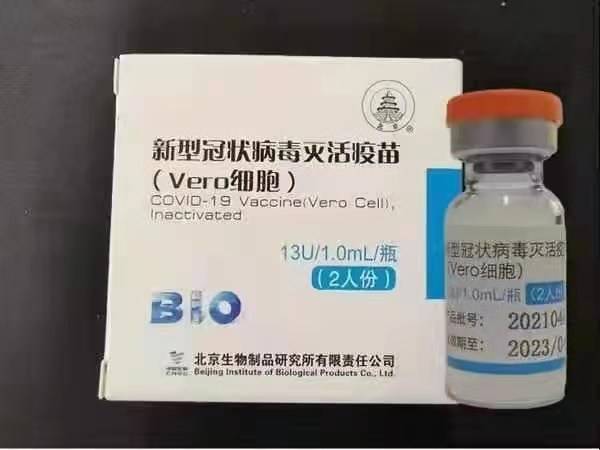
Sinopharm (Πεκίνο): BBIBP-CorV
ΦΑΣΗ 1
1 Δοκιμή
ChiCTR2000032459
Κίνα
ΦΑΣΗ 2
2 Δοκιμές
NCT04962906
Αργεντίνη
ChiCTR2000032459
Κίνα
ΦΑΣΗ 3
6 Δοκιμές
NCT04984408
ChiCTR2000034780
Ηνωμένα Αραβικά Εμιράτα
NCT04612972
Περού
NCT04510207
Μπαχρέιν, Αίγυπτος, Ιορδανία, Ηνωμένα Αραβικά Εμιράτα
NCT04560881, BIBP2020003AR
Αργεντίνη
NCT04917523
Ηνωμένα Αραβικά Εμιράτα
Εγκρίσεις
Λίστα χρήσεων έκτακτης ανάγκης ΠΟΥ 59 χώρες
Αγκόλα 、 Αργεντινή 、 Μπαχρέιν 、 Μπαγκλαντές 、 Λευκορωσία 、 Μπελίζ 、 Βολιβία (Plurinational State of) 、 Βραζιλία 、 Μπρουνέι Νταρουσαλάμ 、 Καμπότζη 、 Καμερούν 、 Τσαντ 、 Κίνα 、 Κομόροι 、 Αίγυπτος 、 Ισημερινή Γουινέα 、 Γκαμπόν 、 Γκάμπια 、 Ουγγαρία 、 Γεωργία 、 Γεωργία 、 Ιράν (Ισλαμική Δημοκρατία του) 、 Ιράκ 、 Ιορδανία 、 Κιργιζία 、 Λαϊκή Δημοκρατία του Λάος
Λίβανος 、 Μαλαισία 、 Μαλδίβες 、 Μαυριτανία ur auritius 、 Μογγολία 、 Μαυροβούνιο 、 Μαρόκο 、 Μοζαμβίκη 、 Ναμίμπια 、 Νεπάλ 、 Νίγηρας 、 Βόρεια Μακεδονία 、 Πακιστάν 、 Παραγουάη 、 Περού 、 Φιλιππίνες 、 Δημοκρατία του Κονγκό 、 Ενεργάλε 、 Σερβιγάλ 、 Σερβία 、 Νησιά 、 Σομαλία ri Σρι Λάνκα 、 Ταϊλάνδη 、 Τρινιδάδ και Τομπάγκο 、 Τυνησία 、 Ηνωμένα Αραβικά Εμιράτα 、 Βενεζουέλα (Δημοκρατία της Βολιβαρίας) 、 Βιετνάμ 、 Ζιμπάμπουε
Το Sinopharm BBIBP-CorV COVID-19 είναι ένα αδρανοποιημένο εμβόλιο κατασκευασμένο από σωματίδια ιού καλλιεργημένα σε καλλιέργεια που στερούνται παθογόνου ικανότητας. Αυτός ο υποψήφιος εμβολίου αναπτύχθηκε από την Sinopharm Holdings και το Ινστιτούτο Βιολογικών Προϊόντων του Πεκίνου.
Το εμβόλιο Sinopharm BBIBP-CorV λειτουργεί επιτρέποντας στο ανοσοποιητικό σύστημα να παράγει αντισώματα κατά του κορωνοϊού βήτα SARS-CoV-2. Τα αδρανοποιημένα εμβόλια ιών χρησιμοποιούνται εδώ και δεκαετίες, όπως το εμβόλιο κατά της λύσσας και το εμβόλιο κατά της ηπατίτιδας Α. Αυτή η τεχνολογία ανάπτυξης έχει εφαρμοστεί με επιτυχία σε πολλά γνωστά εμβόλια, όπως το εμβόλιο κατά της λύσσας.
Το στέλεχος SARS-CoV-2 του Sinopharm (στέλεχος WIV04 και αριθμός βιβλιοθήκης MN996528) απομονώθηκε από έναν ασθενή στο νοσοκομείο Jinyintan στο Wuhan της Κίνας. Ο ιός πολλαπλασιάστηκε σε καλλιέργεια σε κατάλληλη κυτταρική σειρά Vero και το υπερκείμενο των μολυσμένων κυττάρων απενεργοποιήθηκε με β-προπιολακτόνη (1: 4000 vol/vol, 2 έως 8 ° C) για 48 ώρες. Μετά τη διαύγαση των κυτταρικών υπολειμμάτων και την υπερδιήθηση, πραγματοποιήθηκε μια δεύτερη αδρανοποίηση της β-προπιολακτόνης υπό τις ίδιες συνθήκες με την πρώτη απενεργοποίηση. Σύμφωνα με τον ΠΟΥ, το εμβόλιο προσροφήθηκε σε 0,5 mg στυπτηρίας και φορτώθηκε σε προγεμισμένες σύριγγες σε 0,5 ml αποστειρωμένου αλατούχου διαλύματος με ρυθμισμένο φωσφορικό άλας χωρίς συντηρητικά.
Στις 31 Δεκεμβρίου 2020, η Κρατική Υπηρεσία Φαρμάκων ανακοίνωσε την έγκριση του πειραματικού εμβολίου που αναπτύχθηκε από την Sinopharm.
Στις 7 Μαΐου 2021, ο Παγκόσμιος Οργανισμός Υγείας ανακοίνωσε την έγκριση του εμβολίου. Ο κατάλογος χρήσης έκτακτης ανάγκης του ΠΟΥ επέτρεψε στις χώρες να επισπεύσουν τις δικές τους κανονιστικές εγκρίσεις για την εισαγωγή και τη διαχείριση του εμβολίου COVID-19. Η συμβουλευτική ομάδα εμπειρογνωμόνων του ΠΟΥ για τις στρατηγικές ανοσοποίησης έχει επίσης ολοκληρώσει την ανασκόπηση του εμβολίου. Με βάση όλα τα διαθέσιμα στοιχεία, ο ΠΟΥ συνιστά δύο δόσεις εμβολίου, με διαφορά τριών έως τεσσάρων εβδομάδων, για ενήλικες 18 ετών και άνω. Η αποτελεσματικότητα του εμβολίου κατά της συμπτωματικής και νοσηλευόμενης νόσου εκτιμάται στο 79% για όλες τις ηλικιακές ομάδες μαζί.
Ο Αμερικανικός Ιατρικός Σύλλογος δημοσίευσε "Μια τυχαία κλινική δοκιμή: Επίδραση 2 αδρανοποιημένων εμβολίων SARS-CoV-2 στη συμπτωματική μόλυνση COVID-19 σε ενήλικες" στις 26 Μαΐου 2021, καταλήγοντας στο συμπέρασμα ότι "σε αυτήν την προκαθορισμένη ενδιάμεση ανάλυση μιας τυχαιοποιημένης κλινικής δοκιμής, ενήλικες Τα 2 αδρανοποιημένα εμβόλια SARS-CoV-2 που χορηγήθηκαν σε αυτήν την προκαθορισμένη ενδιάμεση ανάλυση τυχαιοποιημένων κλινικών δοκιμών μείωσαν σημαντικά τον κίνδυνο συμπτωματικής COVID-19 και σπάνια ήταν ανεπιθύμητα συμβάντα. " Σε αυτή τη φάση 3 τυχαιοποιημένη δοκιμή σε ενήλικες, η αποτελεσματικότητα των 2 απενεργοποιημένων εμβολίων ολόκληρου του ιού σε συμπτωματικά περιστατικά COVID-19 ήταν 72,8% και 78,1%, αντίστοιχα. 2 εμβόλια είχαν σπάνιες σοβαρές ανεπιθύμητες ενέργειες με παρόμοια συχνότητα με την ομάδα ελέγχου μόνο για στυπτηρία και τα περισσότερα δεν σχετίζονται με τον εμβολιασμό. Μια διερευνητική ανάλυση διαπίστωσε ότι τα 2 εμβόλια προκάλεσαν μετρήσιμα εξουδετερωτικά αντισώματα, παρόμοια με τα αποτελέσματα της δοκιμής φάσης 1/2.
Η ομάδα εργασίας WHO SAGE δημοσίευσε μια ανασκόπηση του εμβολίου Sinopharm/BBIBP COVID-19 στις 10 Μαΐου 2021. Το εμβόλιο COVID-19 του GAVI ενσωματώνει ένα φιαλίδιο εμβολίου που ενημερώνει τους εργαζόμενους υγείας εάν το εμβόλιο έχει αποθηκευτεί σωστά και δεν έχει εκτεθεί υπερθέρμανση. Ως αποτέλεσμα, ζημιά, ανέφερε η GAVI στις 14 Μαΐου 2021. Οι έξυπνες ετικέτες που κατασκευάστηκαν από τη Zebra Technologies και κατασκευάστηκαν από την Temptime Corporation, αποτελούνται από έναν κύκλο με ένα πιο ανοιχτόχρωμο τετράγωνο στη μέση, κατασκευασμένο από ένα άχρωμο χημικό που αναπτύσσει μη αναστρέψιμα το χρώμα με την πάροδο του χρόνου Το Αυτό γίνεται πιο σκοτεινό για να δώσει μια οπτική ένδειξη της αθροιστικής έκθεσης στη θερμότητα. Μόλις το φιαλίδιο εκτίθεται σε θερμότητα πέρα από το βέλτιστο εύρος αποθήκευσης, το τετράγωνο γίνεται πιο σκούρο από τον κύκλο, υποδεικνύοντας ότι το εμβόλιο δεν πρέπει να χρησιμοποιείται πλέον.
Αριθμός εγγραφής βιβλιοθήκης φαρμάκων εθνικού φαρμάκου BBIBP-CorV εμβολίου COVID-19: DB15807.